Новые исследования раскрывают критическую причину, по которой противораковые методы лечения не эффективны для всех пациентов: лекарства накапливаются неравномерно внутри опухолей, часто застревая в клеточных «центрах переработки» под названием лизосомы. Это открытие объясняет, почему некоторые раковые клетки получают смертельную дозу лекарства, в то время как другие почти не затронуты, даже когда пациенты получают одинаковое лечение.
Проблема Современных Противораковых Препаратов
Недавние достижения в лечении рака, включая препараты, такие как ингибиторы PARP (эффективно используемые при раке яичников), улучшили результаты. Однако значительное число пациентов либо не реагирует на эти лекарства, либо развивает устойчивость со временем. Ключевой вопрос заключается не только в том, достигает ли лекарство опухоли, но и в том, как оно распространяется внутри опухоли и отдельных раковых клеток.
Исследователи из Имперского колледжа Лондона непосредственно наблюдали этот процесс, используя тонкие срезы реальных человеческих опухолей яичников, сохраненных в лаборатории в живом состоянии. Обрабатывая эти «экспланты» ингибиторами PARP, они могли отслеживать движение лекарств через фактическую ткань опухоли.
Картографирование Распределения Лекарств С Помощью Продвинутой Визуализации
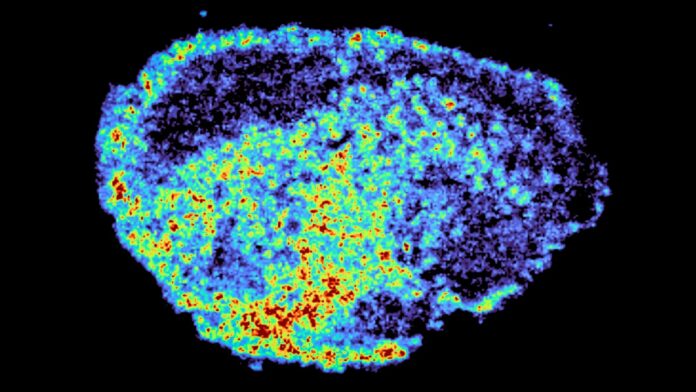
Команда использовала две мощные методики для визуализации поглощения лекарств: масс-спектрометрическую визуализацию (для определения мест накопления лекарств) и пространственную транскриптомику (для измерения активности генов в областях с высоким и низким содержанием лекарств). Результаты показали огромную вариабельность в распределении лекарств, даже среди пациентов, получающих одинаковую дозу.
«Новым аспектом этого исследования было использование масс-спектрометрической визуализации для прямого измерения и визуализации поглощения лекарств в ткани опухоли пациента. С помощью пространственного картографирования молекул лекарств мы могли точно определить области с высоким и низким содержанием лекарств и сравнить экспрессию генов, из одного и того же среза ткани, с помощью пространственной транскриптомики». – Доктор Зои Холл
Лизосомы: Скрытые Резервуары Лекарств
Исследование выявило лизосомы как ключевых игроков в этом неравномерном распределении. Эти клеточные структуры предназначены для расщепления отходов, но некоторые ингибиторы PARP застревают внутри них, превращая их в резервуары медленного высвобождения.
Это означает, что некоторые раковые клетки получают длительное воздействие лекарства, в то время как другие остаются в значительной степени нетронутыми. Исследование показало, что этот эффект более выражен у некоторых лекарств (таких как рукапариб и нирапариб), чем у других (таких как олапариб).
«Мы были удивлены, увидев большую вариабельность накопления лекарств на уровне отдельных клеток. Эта вариабельность была обусловлена накоплением лекарств в лизосомах, которые действуют как резервуары, увеличивая воздействие лекарств на раковые клетки за счет хранения и высвобождения лекарства при необходимости». – Доктор Кармен Рамирес Монкайя
Последствия для Персонализированного Лечения Рака
Ингибиторы PARP уже используются для лечения рака яичников, молочной железы и предстательной железы, с продолжающимися испытаниями в других типах рака. Понимание того, как лекарства хранятся внутри клеток, может привести к более персонализированному лечению, которое максимизирует эффективность и минимизирует устойчивость.
Исследователи надеются выявить биомаркеры в опухоли пациента, которые предскажут, как будут распределяться лекарства, что позволит им адаптировать терапию соответствующим образом.
Будущие исследования будут сосредоточены на том, как доставка лекарств через кровоток, структура опухоли и хранение в лизосомах взаимодействуют у реальных пациентов. Это крайне важно, поскольку опухоли в организме имеют беспорядочные кровеносные сосуды, которые могут ухудшить неравномерное распределение лекарств.
Это исследование подчеркивает сложность лечения рака и необходимость точной медицины. Решая основные причины, по которым лекарства не работают, ученые могут приблизиться к более эффективным методам лечения для всех пациентов.
Исследование финансировалось Медицинским исследовательским советом, Cancer Research UK, партнерством по подготовке специалистов в области интегративной токсикологии и глобальным фондом Victoria’s Secret для борьбы с раком у женщин.