Nieuw onderzoek onthult een cruciale reden waarom kankerbehandelingen niet voor elke patiënt werken: medicijnen stapelen zich ongelijkmatig op in tumoren en komen vaak vast te zitten in cellulaire ‘recyclingcentra’ die lysosomen worden genoemd. Deze ontdekking verklaart waarom sommige kankercellen een dodelijke dosis medicatie krijgen, terwijl andere nauwelijks worden beïnvloed, zelfs als patiënten dezelfde behandeling krijgen.
Het probleem met de huidige kankermedicijnen
Recente ontwikkelingen op het gebied van de behandeling van kanker, waaronder geneesmiddelen zoals PARP-remmers (die effectief worden gebruikt bij eierstokkanker), hebben de resultaten verbeterd. Een aanzienlijk aantal patiënten reageert echter niet op deze medicijnen of ontwikkelt in de loop van de tijd resistentie. De sleutel is niet alleen of een medicijn een tumor bereikt, maar hoe het zich verspreidt binnen de tumor en individuele kankercellen.
Onderzoekers van het Imperial College London observeerden dit proces rechtstreeks met behulp van dunne plakjes echte menselijke eierstoktumoren die in het laboratorium in leven werden gehouden. Door deze ‘explantaten’ te behandelen met PARP-remmers, konden ze de beweging van de medicijnen door feitelijk tumorweefsel volgen.
Geneesmiddelendistributie in kaart brengen met geavanceerde beeldvorming
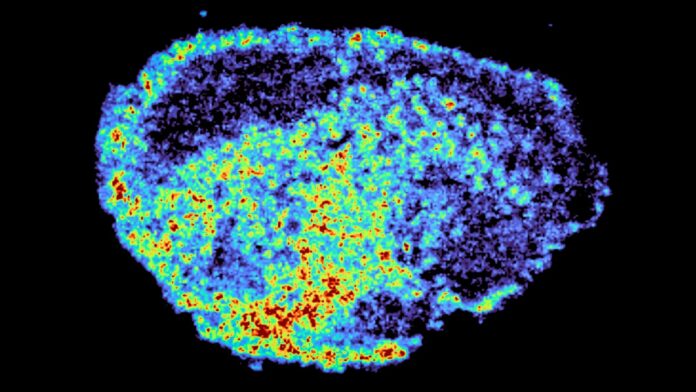
Het team gebruikte twee krachtige technieken om de opname van medicijnen in beeld te brengen: massaspectrometriebeeldvorming (om in kaart te brengen waar medicijnen zich ophopen) en ruimtelijke transcriptomics (om genactiviteit te meten in gebieden met veel en weinig medicijnen). De resultaten lieten een enorme variatie zien in de distributie van geneesmiddelen, zelfs tussen patiënten die dezelfde dosis kregen.
“Een nieuw aspect van deze studie was het gebruik van massaspectrometrie-beeldvorming om de opname van geneesmiddelen in tumorweefsel van patiënten direct te meten en te visualiseren. Door het ruimtelijk in kaart brengen van geneesmiddelmoleculen konden we gebieden met een hoog en laag geneesmiddel aanwijzen en genexpressie vergelijken, uit hetzelfde weefselsegment, met behulp van ruimtelijke transcriptomics.” – Dr. Zoe Hall
Lysosomen: verborgen medicijnreservoirs
Het onderzoek identificeerde lysosomen als sleutelspelers in deze ongelijke verdeling. Deze cellulaire structuren zijn ontworpen om afval af te breken, maar sommige PARP-remmers raken erin gevangen, waardoor ze in reservoirs met langzame afgifte veranderen.
Dit betekent dat sommige kankercellen langdurig aan het medicijn worden blootgesteld, terwijl andere grotendeels onaangetast blijven. Uit de studie bleek dat dit effect bij bepaalde geneesmiddelen (zoals rucaparib en niraparib) meer uitgesproken is dan bij andere (zoals olaparib).
“We waren verrast door de grote variabiliteit in de accumulatie van medicijnen op het niveau van één cel. Deze variabiliteit werd veroorzaakt door de opbouw van een medicijn in de lysosomen, die als reservoirs fungeren en de blootstelling van kankercellen aan medicijnen vergroten, door het medicijn op te slaan en vrij te geven wanneer dat nodig is.” – Dr. Carmen Ramirez Moncayo
Implicaties voor gepersonaliseerde kankerbehandeling
PARP-remmers worden al gebruikt voor de behandeling van eierstok-, borst- en prostaatkanker, terwijl er lopende onderzoeken zijn bij andere soorten kanker. Inzicht in hoe medicijnen in cellen worden opgeslagen, zou kunnen leiden tot meer gepersonaliseerde behandelingen die de effectiviteit maximaliseren en de resistentie minimaliseren.
Onderzoekers hopen biomarkers in de tumor van een patiënt te identificeren die voorspellen hoe medicijnen zich zullen verspreiden, waardoor ze de therapie daarop kunnen afstemmen.
Toekomstig onderzoek zal zich richten op de interactie van medicijnafgifte via de bloedbaan, tumorstructuur en lysosomale opslag bij echte patiënten. Dit is van cruciaal belang omdat tumoren in het lichaam ongeorganiseerde bloedvaten hebben, wat de ongelijkmatige distributie van geneesmiddelen zou kunnen verergeren.
Deze studie onderstreept de complexiteit van de behandeling van kanker en de noodzaak van precisiegeneeskunde. Door de onderliggende redenen aan te pakken waarom medicijnen falen, kunnen wetenschappers dichter bij effectievere therapieën voor alle patiënten komen.
Het onderzoek werd gefinancierd door de Medical Research Council, Cancer Research UK, het Integrative Toxicology Training Partnership en het Victoria’s Secret Global Fund for Women’s Cancers.