De nouvelles recherches révèlent une raison essentielle pour laquelle les traitements contre le cancer ne fonctionnent pas pour tous les patients : les médicaments s’accumulent de manière inégale dans les tumeurs, restant souvent piégés dans des « centres de recyclage » cellulaires appelés lysosomes. Cette découverte explique pourquoi certaines cellules cancéreuses reçoivent une dose mortelle de médicament tandis que d’autres sont à peine affectées, même lorsque les patients reçoivent le même traitement.
Le problème des médicaments anticancéreux actuels
Les progrès récents dans le traitement du cancer, notamment les médicaments comme les inhibiteurs de PARP (utilisés efficacement dans le cancer de l’ovaire), ont amélioré les résultats. Cependant, un nombre important de patients ne répondent pas à ces médicaments ou développent une résistance avec le temps. La clé n’est pas seulement si un médicament atteint une tumeur, mais comment il se propage à l’intérieur de la tumeur et des cellules cancéreuses individuelles.
Des chercheurs de l’Imperial College de Londres ont observé directement ce processus en utilisant de fines tranches de véritables tumeurs ovariennes humaines conservées en vie en laboratoire. En traitant ces « explants » avec des inhibiteurs de PARP, ils pourraient suivre le mouvement des médicaments à travers le tissu tumoral réel.
Cartographie de la distribution des médicaments grâce à l’imagerie avancée
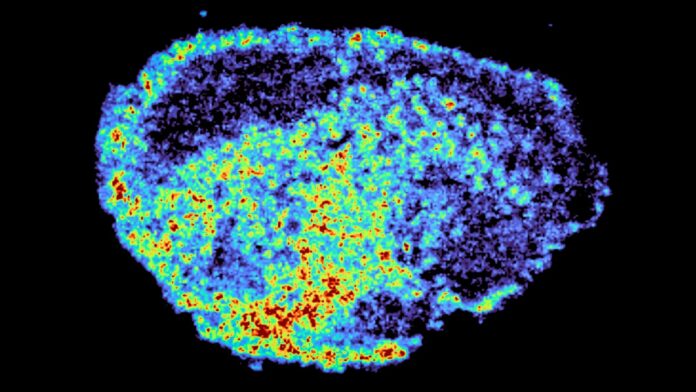
L’équipe a utilisé deux techniques puissantes pour visualiser l’absorption des médicaments : l’imagerie par spectrométrie de masse (pour cartographier l’endroit où les médicaments s’accumulent) et la transcriptomique spatiale (pour mesurer l’activité des gènes dans les zones à forte et faible consommation de médicaments). Les résultats ont montré une énorme variabilité dans la distribution des médicaments, même entre les patients recevant la même dose.
“Un nouvel aspect de cette étude était l’utilisation de l’imagerie par spectrométrie de masse pour mesurer et visualiser directement l’absorption du médicament dans le tissu tumoral du patient. Grâce à la cartographie spatiale des molécules médicamenteuses, nous avons pu identifier les régions à concentration élevée et faible de médicament et comparer l’expression des gènes, à partir de la même tranche de tissu, en utilisant la transcriptomique spatiale.” – Dr Zoé Hall
Lysosomes : des réservoirs cachés de médicaments
La recherche a identifié les lysosomes comme acteurs clés de cette répartition inégale. Ces structures cellulaires sont conçues pour décomposer les déchets, mais certains inhibiteurs de PARP restent piégés à l’intérieur, les transformant en réservoirs à libération lente.
Cela signifie que certaines cellules cancéreuses subissent une exposition prolongée au médicament tandis que d’autres restent largement inchangées. L’étude a révélé que cet effet est plus prononcé avec certains médicaments (comme le rucaparib et le niraparib) qu’avec d’autres (comme l’olaparib).
“Nous avons été surpris de constater une grande variabilité dans l’accumulation de médicaments au niveau cellulaire. Cette variabilité était due à l’accumulation d’un médicament dans les lysosomes, qui agissent comme des réservoirs, augmentant l’exposition des cellules cancéreuses aux médicaments, en stockant et en libérant le médicament en cas de besoin.” – Dr Carmen Ramírez Moncayo
Implications pour le traitement personnalisé du cancer
Les inhibiteurs de PARP sont déjà utilisés pour traiter les cancers de l’ovaire, du sein et de la prostate, et des essais sont en cours sur d’autres types de cancer. Comprendre comment les médicaments sont stockés à l’intérieur des cellules pourrait conduire à des traitements plus personnalisés qui maximiseraient l’efficacité et minimiseraient la résistance.
Les chercheurs espèrent identifier des biomarqueurs dans la tumeur d’un patient qui prédisent la manière dont les médicaments se distribueront, leur permettant ainsi d’adapter le traitement en conséquence.
Les recherches futures se concentreront sur la manière dont l’administration de médicaments par la circulation sanguine, la structure tumorale et le stockage lysosomal interagissent chez de vrais patients. Ceci est crucial car les tumeurs du corps ont des vaisseaux sanguins désorganisés, ce qui pourrait aggraver la distribution inégale des médicaments.
Cette étude souligne la complexité du traitement du cancer et la nécessité d’une médecine de précision. En s’attaquant aux raisons sous-jacentes de l’échec des médicaments, les scientifiques peuvent se rapprocher de thérapies plus efficaces pour tous les patients.
La recherche a été financée par le Medical Research Council, Cancer Research UK, l’Integrative Toxicology Training Partnership et le Victoria’s Secret Global Fund for Women’s Cancers.